心臓発作は、世界の主要な死因の一つです。3D微細造形により、ライフサイエンスの研究を、この分野の病気を治すための再生医療へ大きく近づけることができます。ボストン大学の科学者たちは、2光子重合(2PP)で製造したマイクロ流体ハートオンチップ・プラットフォームでこの目標に貢献しました。これにより、心臓組織の基礎研究への道が開かれ、最終的には拍動している心臓に埋め込むことが出来る組織の製造が可能となります。
心臓病やドラッグデリバリーの研究を推進する3D造形したハートオンチップ
組織パッチを製造し、心臓などの臓器に組み込むことができることを想像してみてください。この想像はメアリー・シェリーの有名な怪奇小説「フランケンシュタイン」のように聞こえるでしょう。しかし実際に、この分野の研究は、何百万人もの患者が深刻な医療問題や病気から回復し、生活の質を取り戻すのに役立ちます。心臓の筋肉組織は、主に心筋細胞から構成されています。心臓発作でこれらの組織は不可逆的に損傷を受け、自己再生することはありません。現在のライフサイエンス研究における野心的目標は、患者自身の幹細胞から機能的なマクロスケールの心臓組織パッチを製造することです。これらの人工的な組織細胞は、心臓発作後に病気や損傷を受けた筋肉の代わりとなり、人々が普通の生活を取り戻すのに役立つでしょう。
ハートオンチップを3Dプリンティング
ボストン大学の科学者たちは、近年、カスタマイズ可能な3D微小環境で心筋組織を研究するために、ソフトおよびメカニカルにアクティブな細胞培養プラットフォームを開発しました。この多機能なツールボックスにより、心臓組織を3D環境で成長させ、チップの垂直壁にある細胞接着部位でその自己組織化を観察できます。内蔵の電子センサーで、培養された心臓細胞の収縮によって生じる力を計測します。さらに、培養組織を受動的に引き伸ばすために、メカニカルアクチュエータをチップに組み込みました。このアクチュエータで、一定の機械的歪みおよび動的歪みが心臓組織に与える影響を調査しました。
スタンダードソフトリソグラフィーと2光子重合の融合
ハートオンチップ・プラットフォームは、マイクロ流体アクチュエータで囲まれた心臓組織を含む内輪シーディングウェルで構成されています。細胞接着部位は、シーディングウェルの垂直壁に直接造形されています。
マイクロ流体アクチュエータは、プラットフォームの重要な要素であり、歪みセンサーとしても機能します。液体が流路を流れると、流路とシーディングウェルの間の薄い仕切りが膨張します。この機械的歪みは、プラットフォームの付着部で成長している培養組織に伝えられます。同時に、薄い仕切り壁の歪みを電子的に記録することもできます。
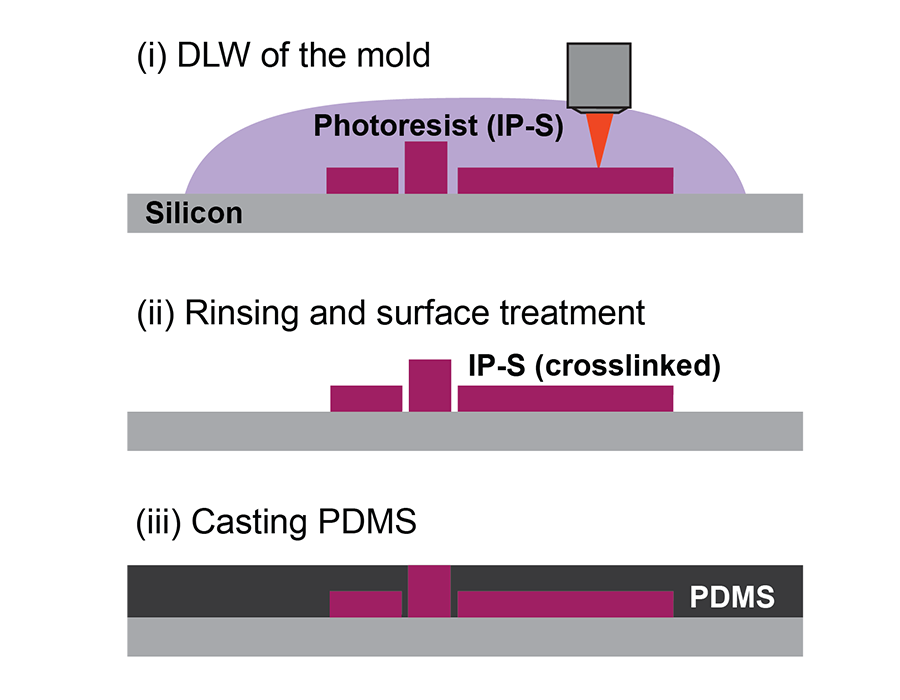
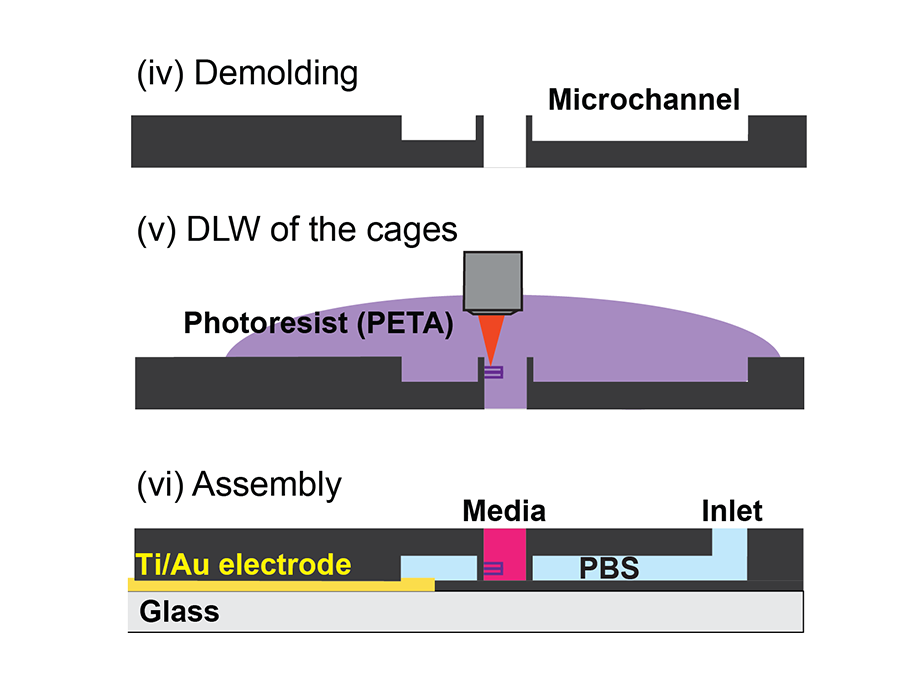
研究チームは、PDMSソフトリソグラフィーを用いてシーディングウェルとそれを取り囲むマイクロ流体チャネルを製作しました。最初に、Nanoscribeの2PP技術を用いてネガティブマスターモールドを作製しました。このレーザー直描により、外側のマイクロ流路と内側のシーディングウェルを隔てる、薄い高アスペクト比のメンブレンウォールを製作出来ました。2PPシステムの真価が発揮されるのは、ネガティブマスターからPDMSシーディングウェルを成形した後です。研究者たちは、再びNanoscribeを使って、カスタマイズした樹脂製のマイクロケージを、シーディングウェルの薄い垂直のメンブレンウォール上に直接造形しました。これらのマイクロ構造は、細胞のアンカーポイントとして機能し、自立した心臓組織の形状を定義します。最後のステップとして、ハートオンチップ・プラットフォームは、電子的な歪みを読み取るための電極接点が組み込まれたガラス基板に接着されます。
心拍同期による先進的な細胞配列の研究
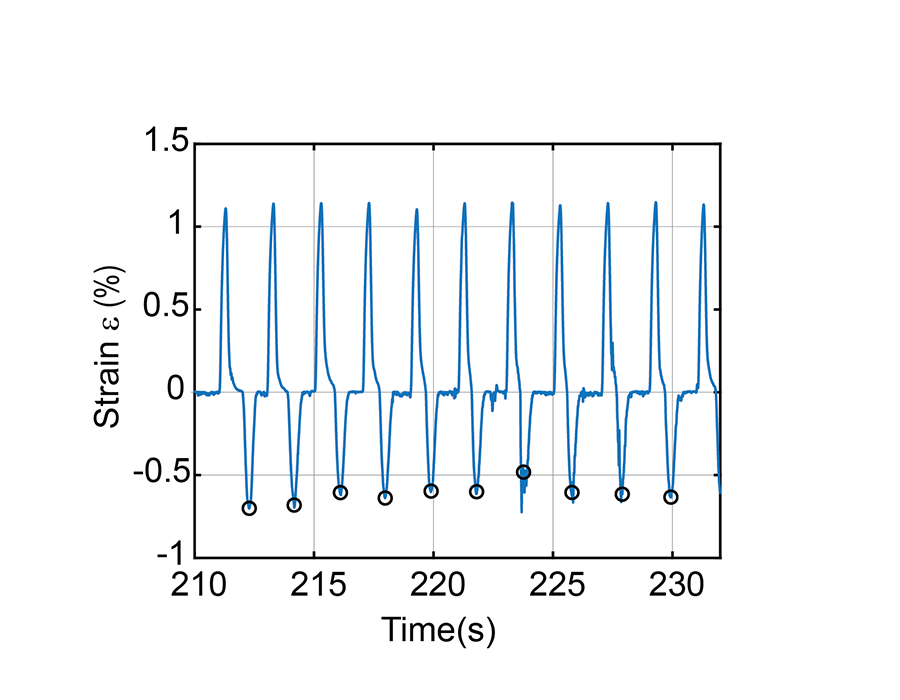
研究者たちは、細胞接着部位の数が異なるプラットフォームを作製し、その位置と数に応じて、シーディングウェル内で自立した心臓組織の形状がどのように変化するかを観察しました。4~5日後、心臓組織が自発的に拍動するようになり、細胞が接着ケージに及ぼす機械的な力を内蔵の歪みセンサーで監視できます。この研究のハイライトは、科学者たちは、マイクロ流体アクチュエータを用いて心臓組織を定期的に引き伸ばしたことです。約3分後、心筋細胞の自発的な収縮が、刺激された拍動と同期しました。この結果、研究者たちはこの組織パッチを拍動する心臓に移植し、患者自身の心臓の拍動に同期させるという目標に一歩近づきました。
組織工学と再生医療の新たな可能性
この目標を達成するには、まだまだ多くの研究が必要です。それでも、研究者たちはNaonscribeの2光子重合技術を用いて、心臓組織に関する詳細な研究と新たな洞察を可能にするプラットフォームを作製することができました。
ボストンの研究者たちが開発したこの新しいハートオンチップ・プラットフォームは、2PPを用いた微細造形が、ライフサイエンス分野のアプリケーションをいかに進化させるかを示す優れた例といえます。生体組織のスケールと2PPベースの3Dプリンティングのサブミクロン精度の解像度は、自然環境を模倣するのに最適です。2PPベースの3Dプリンティングのための生体適合性材料の開発と合わせて、組織工学、細胞生物学、再生医療における他の多くの刺激的なアプリケーションへの応用が期待できます。
Nanoscribeは、BICOグループの一員として、ライフサイエンスの分野における3D微細造形のニーズを予測し、IP-PDMSや、パートナーであるXpect Inx社との共同開発によりN100バイオマテリアルインクなどのプリンティング材料を発売してきました。今後のより刺激的な開発にご期待ください。
この刺激的なプロジェクトについて、さらなる詳細情報にご興味がおありですか?学術論文の全文はこちらからお読みください:Direct laser writing for cardiac tissue engineering: A microfluidic heart on a chip with integrated transducers

上記を含む何百もの研究プロジェクトについての科学出版物は、Premium Resourcesのキーワード検索を利用して、強力なデータベースで検索できます。無料登録で、Nanoscribeの3D微細造形技術による革新的なアプリケーションや、多くの分野にわたる抜本的な技術革新の可能性を探求できます。
動画情報
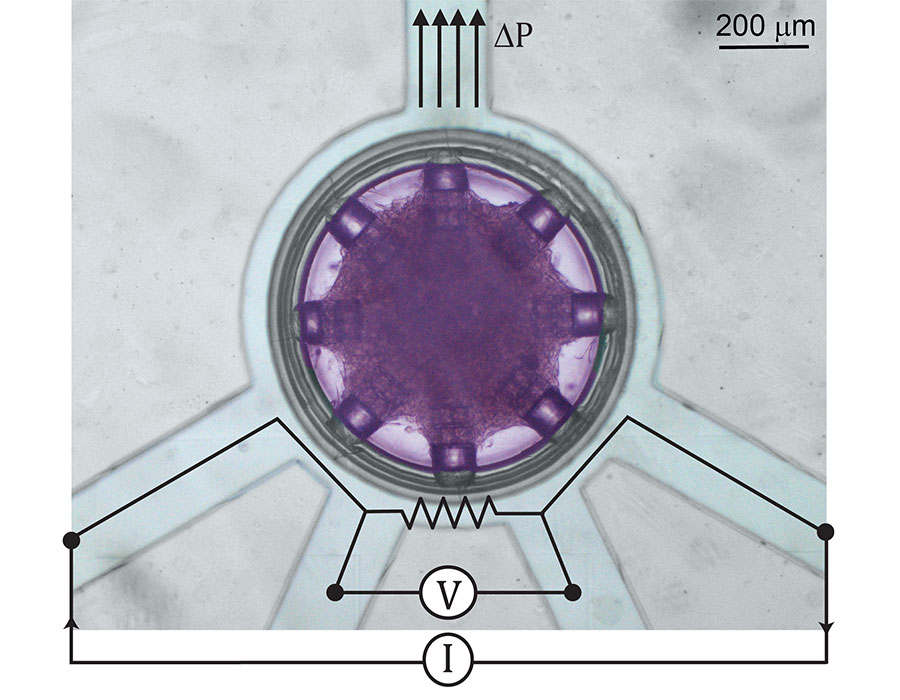
心臓組織を搭載した8つの細胞接着部位を持つハートオンチップ・プラットフォームを顕微鏡から見た図。組織は造形した微細構造に沿って整列し、刺激した拍動に自発的な収縮を同期させます。
Video: M. Çağatay Karakan, Boston University

